在胚胎发育与干细胞研究领域,氧气含量被认为是调控干细胞命运的重要环境因素。已有研究表明低氧及其关键因子HIF-1α可以影响干细胞的多潜能性,但过往研究多集中于其在低氧条件下的功能,而很少关注HIF-1α在不同氧状态下是否具有差异化的转录调节能力,及其对多潜能性维持的阶段特异性作用机制尚未阐明。
针对这一科学问题,沈小鹏副教授课题组以小鼠胚胎干细胞(mESCs)为研究对象,系统探究了HIF-1α在从常氧到低氧过渡过程中对基因组结合和多潜能性调控的阶段特异性作用。研究利用染色质免疫沉淀测序(ChIP-Seq)和转录组测序(RNA-Seq),发现HIF-1α在氧气过渡过程中表现出独特的“结合–释放–再结合”模式,导致其在常氧和稳定低氧阶段维持多潜能性基因表达,但在急性低氧过渡阶段反而失去调控能力。此外,研究还发现HIF-1α通过调节LIF受体(LIFR)及其下游JAK-STAT信号通路,在不同氧环境下以阶段特异性方式维系干细胞多潜能性。该研究揭示了HIF-1α调节干细胞多潜能性的动态基因组调控机制,有助于理解氧感应与多潜能性维持之间的关系,并为干细胞稳态调控和再生医学应用提供新视角。
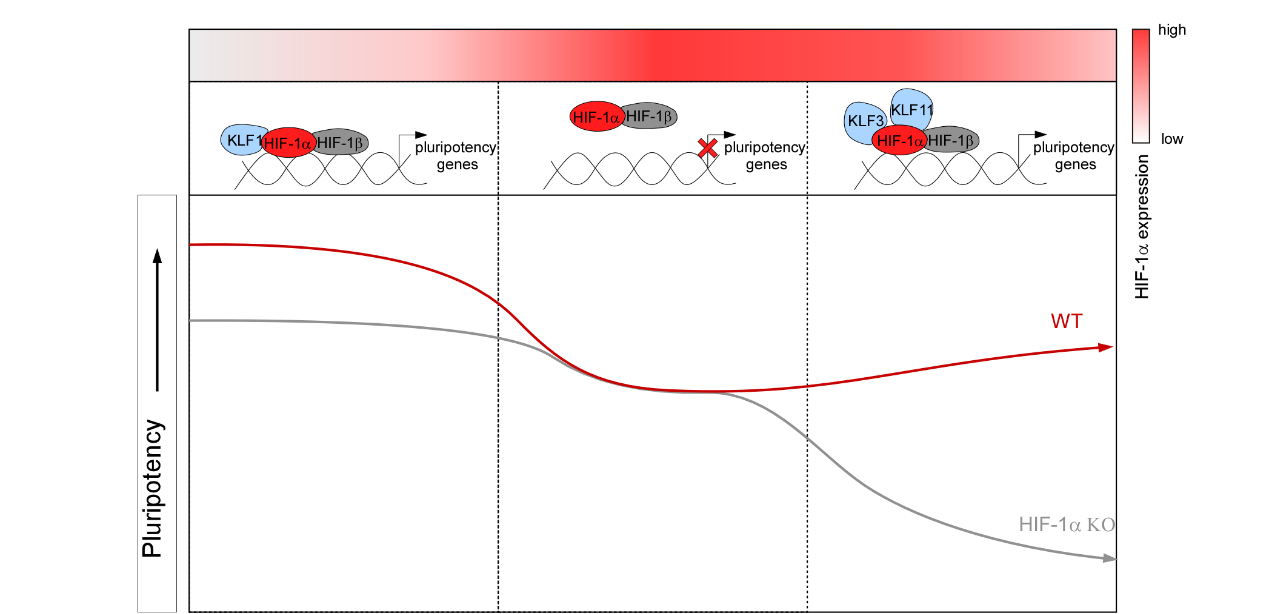
图:HIF-1α在不同氧状态下对mESCs多潜能性维持的影响
相关研究以“The stage-specific roles of HIF-1α in regulating mESC pluripotency during oxygen transition”为题,发表在生物化学与分子生物学领域国际著名期刊《Journal of Biological Chemistry》。皇冠新款入口为论文第一完成单位,博士生李蒙为论文第一作者,沈小鹏为通讯作者。研究还得到了浙江大学、皖南医学院等多家单位学者的合作支持。
原文链接:https://doi.org/10.1016/j.jbc.2025.110344

